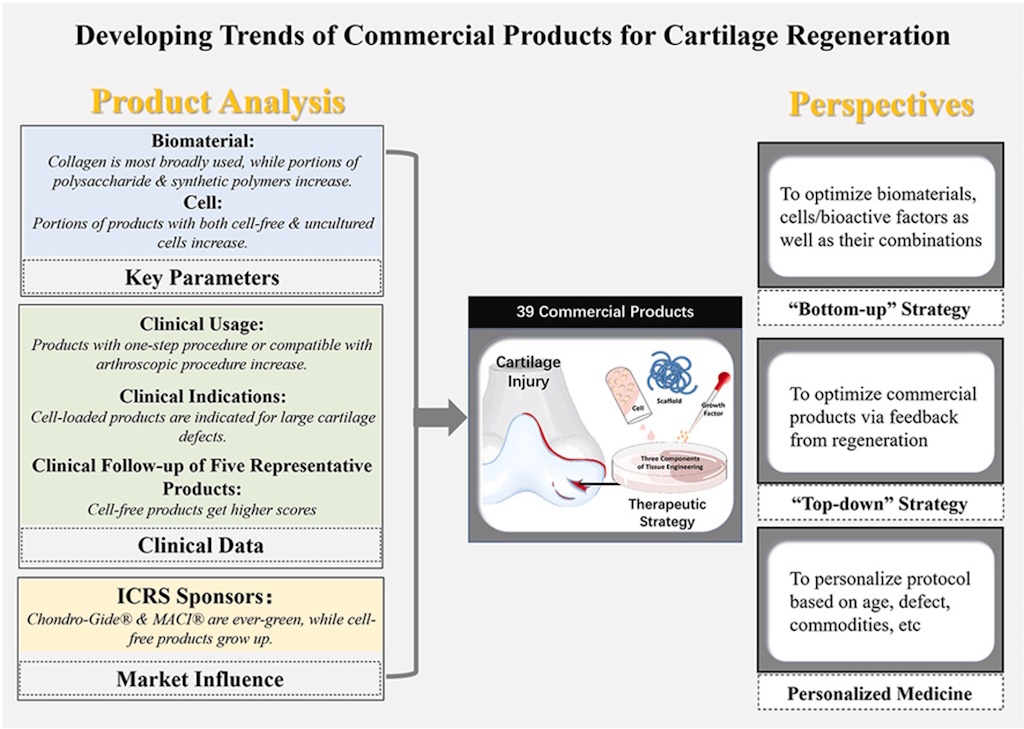
Gráfico de un cuarto de siglo de productos comerciales para la regeneración del cartílago

Resumen
La regeneración
funcional del cartílago sigue siendo difícil de lograr a pesar de
décadas de investigación. Se han propuesto docenas de productos
comerciales, cada uno de los cuales se centra en diferentes facetas de
la ingeniería exitosa del cartílago, incluidas las propiedades
mecánicas, la integración, la lubricación y la inflamación; sin embargo,
sigue habiendo una falta de avances en resultados clínicos
significativos. Las investigaciones anteriores clasificaron los
productos comerciales en función de sus componentes y aclararon los
desafíos que se enfrentaron durante el proceso de aprobación del
mercado. Este artículo, por primera vez, revisa exhaustivamente las
propiedades de los productos comerciales que abarcan los últimos 25
años, incluidas las tendencias de diseño de los componentes, la
compatibilidad con la cirugía mínimamente invasiva, las indicaciones
para los defectos del cartílago, el seguimiento a largo plazo, así como
el apoyo activo del patrocinio de la Sociedad Internacional de
Regeneración del Cartílago y Preservación de las Articulaciones (ICRS).
Nuestro objetivo es resumir los factores clave para los productos
comerciales potencialmente exitosos y dilucidar las tendencias generales
en el desarrollo de tecnología en este campo. Dado que ningún producto
revolucionario ha producido resultados clínicos significativamente
mejorados, los productos emergentes compiten entre sí en cuanto a
facilidad de uso y relación costo-beneficio. Otras características
relevantes incluyen la compatibilidad con la cirugía mínimamente
invasiva, la extensión de la cirugía requerida (una etapa frente a dos
etapas), el uso de polímeros artificiales versátiles y la aplicación de
células y biomateriales. Algunos productos específicos continúan
liderando el mercado debido a su relación costo-beneficio o indicaciones
para defectos de cartílago más grandes. Sin embargo, se ha demostrado
que no producen una mejora significativa en el seguimiento clínico. Por
lo tanto, existe la necesidad de productos que superen a los productos
comerciales actuales y muestren eficacia clínica.
Potencial de
traducción de este artículo: Esta revisión analiza los componentes del
producto, la compatibilidad con la cirugía mínimamente invasiva, la
indicación para áreas con defectos de cartílago, el rendimiento clínico y
el patrocinio de la Conferencia Mundial de la Sociedad Internacional de
Regeneración de Cartílago y Preservación de Articulaciones, basándose
en información sobre productos de regeneración de cartílago desde 1997
hasta 2023. Arroja luz sobre el desarrollo futuro del diseño y la
comercialización de productos de cartílago.
Introducción
La
regeneración funcional del cartílago sigue siendo difícil de alcanzar a
pesar de los importantes esfuerzos de investigación y desarrollo de
productos [1]. Se han propuesto varias estrategias en los esfuerzos por
mejorar la regeneración del cartílago, que incluyen, entre otras, la
reconstrucción de la estructura de colágeno y otras propiedades
mecánicas [2], el ajuste fino de la respuesta inmunológica [3] y la
mejora del potencial de diferenciación de las células madre implantadas
[4]. Los enfoques para dichas estrategias han incluido la eliminación de
células senescentes [5], el uso de la molécula pequeña kartogenina [3],
la estimulación piezoeléctrica [6], la hialinización del fibrocartílago
con estabilización de microtúbulos [7] y el rejuvenecimiento de la
matriz extracelular descelularizada (dECM) [8], todos los cuales han
demostrado una regeneración eficaz del cartílago, al menos en modelos
preclínicos. Sin embargo, siguen existiendo desafíos que impiden la
traducción clínica [6]. Se han desarrollado múltiples productos y
tecnologías comerciales, que han recibido la aprobación regulatoria y se
han utilizado en aplicaciones clínicas [7,9]; sin embargo, ninguno de
estos productos ha logrado una mejora clínicamente significativa a largo
plazo. Con los desafíos que enfrenta actualmente este campo, nos
esforzamos por investigar las posibles razones subyacentes a estos
resultados clínicos mediocres mediante el seguimiento de las tendencias
en desarrollo para proporcionar fundamentos y orientación para la mejora
futura de los productos comerciales y la tecnología.
La regeneración
del cartílago es un proceso complejo y técnicamente desafiante. Visto
desde sus propiedades materiales, el cartílago no solo está compuesto
por una proporción equilibrada de colágeno/glicosaminoglicano y subtipos
de colágenos, sino también por un conjunto afinado de fibrillas de
colágeno, fibras, haces y enlaces cruzados [10]. En biología
regenerativa, los condrocitos y las células progenitoras son
responsables de la producción y el mantenimiento de la matriz
extracelular del cartílago, que explica su función fisiológica dinámica.
Estas funciones son muy sensibles al microambiente celular circundante;
cualquier cambio en la ósmosis, el valor del pH, los iones, las
citocinas y los factores de crecimiento a menudo pueden ser
perjudiciales después de una lesión del cartílago [2]. A medida que el
cartílago articular se desarrolla y funciona en condiciones hipóxicas,
la presencia de aire (en caso de lesión articular abierta) o sangre en
la articulación (ya sea de los tejidos circundantes o de la fisura del
cartílago y el hueso subcondral) inevitablemente alteraría este
microambiente. Además, la integración exitosa del cartílago regenerado
es de gran importancia, pero también es un desafío de llevar a cabo y, a
menudo, se ignora durante la ingeniería del producto. Muy a menudo, los
productos existentes regeneran el «cartílago» que contiene colágeno
tipo II en lugar del cartílago hialino predominantemente de colágeno
tipo II, que contiene entre dos y tres por ciento de colágeno de tipos
I/III [2]. Los complejos mecanismos terapéuticos de estos productos de
ingeniería tisular siguen siendo desconocidos, por lo que no es
sorprendente que conduzcan a una regeneración funcional subóptima del
cartílago. Lograr resultados clínicos favorables a largo plazo depende
de la intrincada interacción de varios factores, en lugar de un avance
en cualquier aspecto individual.
Durante los últimos treinta años, se
han revisado en profundidad las ventajas y desventajas de las
tecnologías de ingeniería tisular para la reparación del cartílago [9];
Las características químicas, físicas y mecánicas de los andamios están
diseñadas para influir en el rendimiento del producto en aplicaciones
clínicas [11]. Como tal, las principales barreras para la traducción
clínica de los productos regenerativos del cartílago articular se
atribuyen a la estructura regulatoria de la Administración de Alimentos y
Medicamentos (FDA) con respecto a la revisión de los productos de
reparación del cartílago, así como las limitaciones a su uso en modelos
animales grandes [6]. Por otro lado, diferentes agencias regulatorias
han aprobado una cantidad relativamente grande de productos comerciales
de regeneración del cartílago con conceptos y enfoques similares [12].
La
literatura anterior que categoriza los componentes de los productos o
tecnologías no ha logrado proporcionar una descripción general completa y
cuantitativa. Además, han surgido nuevos productos comerciales,
incluidos CartiLife® (Biosolution), Agili-C® (CartiHeal) y Prochondrix®
(Stryker), que consisten en pequeñas perlas, andamios de dos fases o
aloinjertos grabados con láser, lo que resalta las tendencias
comerciales en el campo. Los productos comerciales de regeneración de
cartílago aprobados por la FDA u otras agencias desde 1995 hasta el
presente se investigan y examinan para detectar posibles cambios en la
composición del producto, la facilidad de uso, los resultados clínicos y
el patrocinio de una sociedad profesional, con la esperanza de ayudar
en el desarrollo de nuevas tecnologías con mejores resultados clínicos.
Perspectivas
El
fortalecimiento de células, biomateriales, factores de crecimiento o su
combinación podrían desarrollar productos comerciales de manera
eficiente a través de una estrategia “de abajo hacia arriba”. Las
células progenitoras de cartílago de diversas fuentes [86,87], las MSC
preparadas con potenciales condrogénicos más altos mediante tratamiento
con campo eléctrico [[88], [89], [90]] y expansión de dECM [91,92], y
los factores de crecimiento diseñados con alta afinidad por la matriz
extracelular o los biomateriales [93,94] promueven significativamente la
regeneración del cartílago. Los biomateriales han sido durante mucho
tiempo componentes vitales de los productos comerciales, aunque no hay
consenso sobre las funciones y los componentes y estructuras óptimos de
los biomateriales utilizados hasta la fecha. Aunque los andamios de
esponja se han adoptado ampliamente, como las esponjas de colágeno
utilizadas en Chondro-Gide® y MACI®, los hidrogeles, como HYALOFSAT®,
han ganado más popularidad debido a la facilidad de uso y los avances
técnicos. Aunque los hidrogeles pueden hacerse duraderos (con un módulo
de Young alto) [95] y versátiles, los hidrogeles utilizados en productos
comerciales generalmente carecen de propiedades mecánicas y otras
propiedades especiales. Los hidrogeles ayudan a mantener los fenotipos
de los condrocitos y promueven la diferenciación condrógena de las MSC,
mientras que las esponjas facilitan la agregación y proliferación
celular, que son fundamentales para la regeneración del cartílago
[96,97].
Una estrategia alternativa para optimizar los productos
comerciales es priorizar la necesidad de propiedades de diseño
específicas utilizando una especie de estrategia «de arriba hacia
abajo». Sin embargo, el conocimiento limitado sobre la biología de la
regeneración del cartílago restringe nuestros esfuerzos para desarrollar
y optimizar productos comerciales. El colágeno y los polisacáridos
podrían facilitar la integración de las células y la matriz
extracelular, apoyar la supervivencia en la etapa inicial de la
regeneración, mejorar el contenido de colágeno y promover la producción
de proteoglicanos. Sin embargo, cada material afecta el comportamiento
celular a través de diferentes mecanismos. La escasa y oscura
comprensión de la relación entre los biomateriales y el cartílago
regenerado limita nuestros esfuerzos por establecer “principios de
diseño” para los biomateriales, tanto por sí mismos como en combinación
con células y factores de crecimiento. Es importante monitorear el
proceso de regeneración, lo que incluye evaluar la degradación de los
biomateriales, el destino de las células trasplantadas y las moléculas
bioactivas, así como los cambios posteriores en el microambiente.
La
medicina precisa o el tratamiento personalizado también se podrían
utilizar en combinación con productos comerciales adoptados
universalmente. Los protocolos de tratamiento personalizados deberían
basarse en la ubicación, el área y la profundidad de los defectos del
cartílago, así como en la edad, las comorbilidades, el estado
inmunológico y el estado metabólico. Es un desafío establecer protocolos
de tratamiento personalizados sin una comprensión sólida de los
mecanismos fundamentales; sin embargo, se pueden utilizar intentos
empíricos en combinación con principios de diseño basados en
mecanismos. Además de los sistemas de puntuación histológica y la
evaluación mediante resonancia magnética, se deberían integrar sistemas
de puntuación subjetivos de los pacientes. En este caso, el aprendizaje
profundo supervisado con datos multimodales podría ser útil.
https://www.sciencedirect.com/science/article/pii/S2214031X24001396
Journal of Orthopaedic Translation
Volume 50, January 2025, Pages 354-363
Review ArticleCharting a quarter-century of commercial cartilage regeneration products
Author links open overlay panelXinyi Liu a
, Xiaolei Guo b
, Yixuan Amy Pei c
, Ming Pei d
, Zigang Ge ae
https://doi.org/10.1016/j.jot.2024.10.009Get rights and content
Under a Creative Commons license
open access
Note: This article is available under the Creative Commons CC-BY-NC-ND license and permits non-commercial use of the work as published, without adaptation or alteration provided the work is fully attributed.
© 2024 Peking university. Published by Elsevier B.V. on behalf of Chinese Speaking Orthopaedic Society.












