https://www.ortopediaoncologicamexico.mx/academia/osteosarcoma-condroblastico/
Osteosarcoma condroblástico
El osteosarcoma es un sarcoma intramedular productor de osteoides de alto grado. Tiene preferencia por los sitios de las placas de crecimiento más proliferativas.1 Ocurren en la metáfisis de los huesos largos, comúnmente con extensión directa a la epífisis y diáfisis adyacentes. Tiene una presentación bimodal, con la mayoría de los casos entre las edades de 14 y 18 años y un segundo pico más pequeño en adultos mayores.2 La superficie bruta de corte depende del tipo y grado de mineralización de la matriz predominante, que puede ser densa, sólida , blanco tostado, parecido al hueso cortical o gris, gomoso o mucoide en el caso del componente cartilaginoso.3 El diagnóstico histomorfológico del osteosarcoma justifica la demostración de formación ósea neoplásica, que puede ser en cualquier cantidad para realizar el diagnóstico. Característicamente, se observan patrones finos o gruesos en forma de encaje o láminas grandes y anchas de hueso compacto formadas por trabéculas coalescentes. El tumor crece siguiendo un patrón permeativo, reemplazando los espacios de la médula, recubriendo y erosionando las trabéculas óseas. Las células tumorales generalmente muestran un marcado pleomorfismo con abundante mitosis. Según la matriz predominante, los osteosarcomas se subdividen en tipos osteoblásticos (76-80%), condroblásticos (10-13%) y fibroblásticos (10%). En el osteosarcoma condroblástico, el componente predominante es el cartílago hialino con atipia citológica grave. El cartílago neoplásico se fusiona con el osteoide maligno y muestra condensación y formación de células tumorales en la periferia de estos nódulos condroides.3,4 Esta característica es beneficiosa en el diagnóstico por biopsia pequeña, donde es necesario diferenciarlo del condrosarcoma. La estadificación se basa en la mayor dimensión del tumor (≤ 8 cm: T1; > 8 cm: T2) y la afectación discontinua del sitio óseo primario (T3). Las metástasis pulmonares, seguidas de las esqueléticas, son los sitios más frecuentes de enfermedad sistémica.3 Por lo tanto, el osteosarcoma de alto grado generalmente se trata con quimioterapia preoperatoria y posoperatoria, y el control local se logra mediante resección quirúrgica con márgenes amplios utilizando técnicas de salvación de la extremidad. La radiación se puede utilizar para tumores irresecables.5 La respuesta histológica a la quimioterapia neoadyuvante sigue siendo uno de los pronósticos más importantes de la supervivencia general y libre de enfermedad, con una necrosis ≥ 90 % definida como una buena respuesta.6
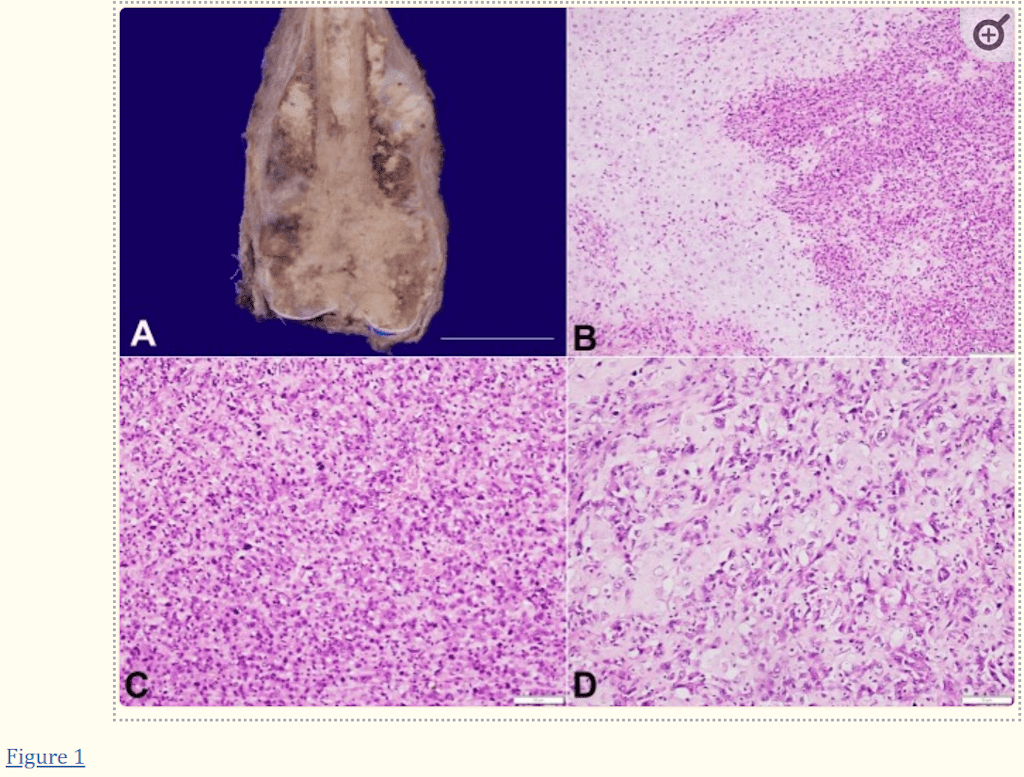
La Figura 1 describe a una mujer de 15 años con hinchazón y dolor en rápido aumento en la pierna izquierda. En la exploración había dolor local y eritema. La tomografía computarizada mostró una lesión lítica destructiva que involucraba la diáfisis y epífisis del extremo femoral inferior con reacción perióstica. También hubo extensión de tejidos blandos y al paciente se le diagnosticó osteosarcoma. Se sometió a quimioterapia con mala respuesta al tratamiento y fue remitido a nuestro centro de atención terciaria para una cirugía de rescate de la extremidad. La muestra extirpada del fémur izquierdo mostró un extremo cóndilar distal expandido. En los bivalvos, se observó un tumor duro de color blanco grisáceo que medía 17,5 × 11,5 × 8,8 cm con áreas variadas de hemorragia, cambio mixoide y calcificación (Figura 1A). Se observó que el tumor se extendía hacia la cavidad medular hasta el cuello. La corteza se rompió con una reacción perióstica y la extensión del tejido blando circundante. Los márgenes articular, de tejidos blandos, muscular y neurovascular estaban libres de tumores. En la microscopía, había láminas, el patrón lobulillar y fascicular del tumor celular se infiltraba en el hueso y el tejido blando (Figura 1B). Las células tumorales mostraron pleomorfismo de moderado a marcado con núcleos vesiculares, nucléolos visibles y una cantidad moderada de citoplasma. Interviniendo las células tumorales, estaba presente una cantidad significativa de depósito de material osteoide similar a un encaje. Se observaron mitosis frecuentes; sin embargo, no se identificó necrosis (Figura 1C). Había nidos y lóbulos de cartílago con mayor celularidad y un marcado grado de atipia nuclear junto con material de matriz osteoide (Figura 1D). Todos los márgenes de resección no estaban afectados por el tumor. Según los hallazgos clínicos, radiológicos e histopatológicos, el diagnóstico de osteosarcoma condroblástico [pT2; manual de estadificación del Comité Conjunto Estadounidense sobre el Cáncer (AJCC); 8ª edición] fue renderizada.
Chondroblastic osteosarcoma – PubMed (nih.gov)
Chondroblastic osteosarcoma – PMC (nih.gov)
Chondroblastic osteosarcoma (autopsyandcasereports.org)
Bhardwaj N, Bachhal V, Saikia UN. Chondroblastic osteosarcoma. Autops Case Rep. 2024 Jan 8;13:e2023466. doi: 10.4322/acr.2023.466. PMID: 38213875; PMCID: PMC10782518.
Copyright © 2023 The Authors.


No hay comentarios:
Publicar un comentario