Antecedentes y objetivos:
La reparación del cartílago
sigue siendo un reto crítico en la medicina ortopédica debido a la
limitada capacidad de autocuración del tejido, lo que contribuye a
enfermedades articulares degenerativas como la osteoartritis (OA). En
respuesta, la medicina regenerativa ha desarrollado estrategias
terapéuticas avanzadas, que incluyen terapias celulares, edición
genética y andamiajes de bioingeniería, para promover la regeneración
del cartílago y restaurar la función articular. Esta revisión narrativa
tiene como objetivo explorar los últimos avances en técnicas de
reparación del cartílago, centrándose en la terapia con células madre
mesenquimales (MSC), las intervenciones genéticas y las innovaciones en
biomateriales. También analiza el impacto de factores específicos del
paciente, como la edad, el tamaño del defecto y la rentabilidad, en la
selección del tratamiento y los resultados. Materiales y métodos: Esta
revisión sintetiza los hallazgos de estudios clínicos y preclínicos
recientes publicados en los últimos cinco años, obtenidos de las bases
de datos PubMed, Scopus y Web of Science. La búsqueda se centró en
términos clave como «reparación de cartílago», «terapia con células
madre», «edición genética», «biomateriales» e «ingeniería tisular».
Resultados: Los avances en terapias basadas en MSC, incluyendo el
implante de condrocitos autólogos (ACI) y el plasma rico en plaquetas
(PRP), han demostrado un prometedor potencial regenerativo. Las
herramientas de edición genética como CRISPR/Cas9 han facilitado
modificaciones celulares dirigidas, mientras que los nuevos
biomateriales como los hidrogeles, los andamios biodegradables y las
construcciones impresas en 3D han mejorado el soporte mecánico y la
integración tisular. Además, los estímulos biofísicos como el
ultrasonido pulsado de baja intensidad (LIPUS) y los campos
electromagnéticos (EMF) han mejorado la diferenciación condrógena y la
producción de matriz. Las decisiones de tratamiento se ven influenciadas
por la edad del paciente, el tamaño del defecto del cartílago y las
consideraciones financieras, lo que destaca la necesidad de enfoques
personalizados y multimodales. Conclusiones: La combinación de técnicas
regenerativas, incluyendo terapias basadas en células, modificaciones
genéticas y andamiaje avanzado, ofrece una vía prometedora hacia la
reparación duradera del cartílago y la preservación articular. Las
investigaciones futuras deberían centrarse en perfeccionar los
protocolos terapéuticos integrados, realizar evaluaciones clínicas a
largo plazo y adoptar modelos de tratamiento personalizados impulsados
por inteligencia artificial y algoritmos predictivos.
Introducción
El
cartílago es un tejido conectivo especializado esencial para la función
articular, proporcionando una superficie lisa y lubricada para la
articulación y una distribución eficaz de la carga. Su naturaleza
avascular y su limitada capacidad intrínseca de reparación lo hacen
particularmente susceptible al daño causado por lesiones o enfermedades
degenerativas, lo que a menudo conduce a disfunción articular progresiva
y osteoartritis (OA), que contribuyen significativamente a la
discapacidad global.
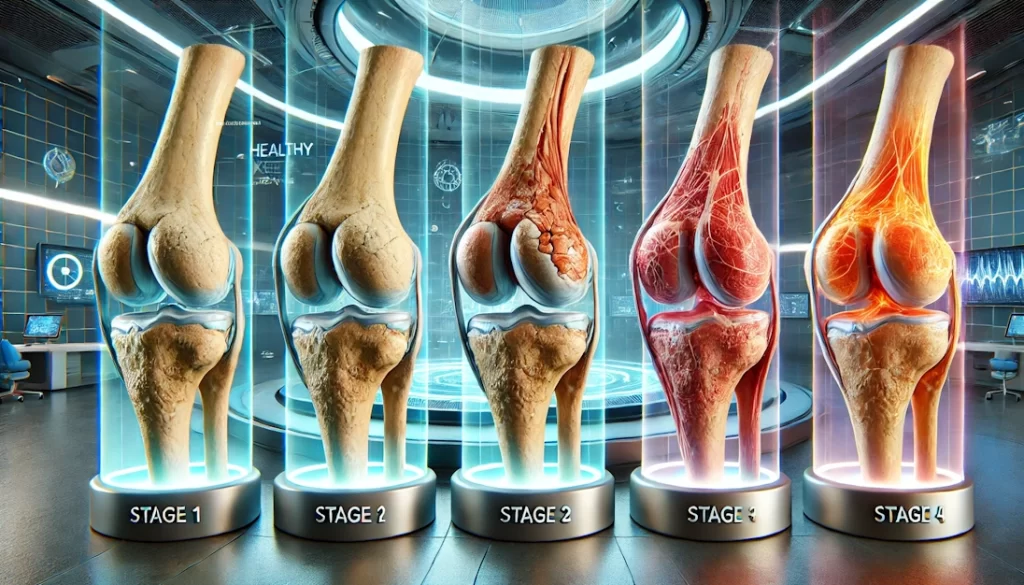
Los mecanismos
morfopatológicos que subyacen al daño del cartílago de la rodilla
implican una compleja interacción de factores mecánicos, bioquímicos y
celulares que conducen a la degradación de la matriz extracelular (MEC).
El estrés mecánico causado por lesiones agudas o el uso excesivo
repetitivo puede alterar la red de colágeno y reducir el contenido de
proteoglicanos, comprometiendo la integridad estructural del cartílago
[1]. Simultáneamente, se sobreexpresan mediadores inflamatorios como las
citocinas y las metaloproteinasas de matriz (MMP), lo que acelera la
degradación de la MEC e inhibe los procesos de reparación [2]. La
apoptosis de los condrocitos disminuye aún más la capacidad del tejido
para el mantenimiento y la regeneración, lo que culmina en el deterioro
progresivo del cartílago y la disfunción articular [3].
Datos epidemiológicos
recientes indican un aumento preocupante de las lesiones del cartílago
de rodilla en personas jóvenes, especialmente en deportistas. Esta
tendencia se atribuye a una mayor participación en deportes de alta
intensidad, lo que conlleva una mayor incidencia de eventos traumáticos
agudos, como desgarros del ligamento cruzado anterior (LCA) y lesiones
meniscales, que a menudo se asocian con daño concomitante del cartílago
[4]. Además, los microtraumatismos repetitivos por sobreuso sin una
recuperación adecuada pueden iniciar cambios degenerativos en el
cartílago [5]. La creciente popularidad de los deportes de alta
intensidad y la participación atlética durante todo el año ha provocado
una exposición más frecuente a estrés mecánico en las articulaciones.
Los períodos de recuperación inadecuados, las técnicas de entrenamiento
inadecuadas y el acceso limitado a programas de medicina deportiva
preventiva agravan aún más el riesgo de lesiones. Asimismo, los avances
en las tecnologías de diagnóstico por imagen han mejorado la detección
del daño del cartílago, lo que ha resultado en una mayor incidencia
reportada. La creciente prevalencia de la obesidad en las poblaciones
jóvenes también contribuye a una mayor carga articular, lo que agrava el
desgaste del cartílago [6]. Estos factores subrayan la necesidad de
estrategias preventivas específicas e intervenciones tempranas para
abordar el daño del cartílago en los grupos demográficos más jóvenes.
Los tratamientos
tradicionales suelen centrarse en el control de los síntomas, mientras
que los enfoques regenerativos buscan restaurar el cartílago dañado a su
estado original. Los avances recientes en medicina regenerativa han
introducido terapias innovadoras destinadas a restaurar la estructura y
la función del cartílago. Las terapias con plasma rico en plaquetas
(PRP) y células madre mesenquimales (MSC) se han convertido en
estrategias no quirúrgicas fundamentales. El PRP aprovecha los factores
de crecimiento para modular la inflamación, estimular la angiogénesis y
mejorar la cicatrización tisular, mientras que las MSC ofrecen
capacidades multipotentes, inmunomodulación y efectos paracrinos para
promover la regeneración del cartílago. Estos enfoques han demostrado
ser prometedores en estudios preclínicos y clínicos iniciales,
demostrando mejoras en el alivio del dolor, la función articular y la
calidad del cartílago [7,8,9].
Sin embargo, la aplicación
clínica de las terapias con PRP y MSC enfrenta desafíos significativos.
La heterogeneidad en los protocolos de preparación de PRP y la obtención
de MSC, junto con la variabilidad en los resultados terapéuticos,
subraya la necesidad de estandarización y optimización [10,11]. Además,
la eficacia del PRP suele verse limitada por su bioactividad de corta
duración, mientras que las terapias con MSC se enfrentan a obstáculos
regulatorios, problemas de escalabilidad y preocupaciones sobre la
seguridad a largo plazo de las intervenciones celulares [12,13].
A pesar de estos avances,
persisten necesidades insatisfechas para lograr una reparación duradera y
reproducible del cartílago. Las terapias actuales a menudo no logran
restaurar el cartílago hialino, el tipo de cartílago nativo, sino que
producen fibrocartílago con propiedades mecánicas y funcionales
inferiores. Además, muchos tratamientos son específicos para cada
estadio y menos efectivos en casos de daño avanzado del cartílago u
osteoartritis, lo que deja una brecha crítica para los pacientes con
degeneración articular grave [14,15].
Estos desafíos resaltan la
necesidad de técnicas regenerativas de nueva generación que aborden las
limitaciones de las terapias existentes. Enfoques novedosos, como las
terapias libres de células basadas en exosomas, los andamiajes de
biomateriales híbridos y las construcciones de cartílago derivadas de
células madre pluripotentes inducidas (iPSC), tienen un inmenso
potencial para superar estas barreras [16]. Estas estrategias buscan
redefinir el panorama de la reparación del cartílago y la preservación
articular mediante la integración de avances en bioingeniería, medicina
de precisión y modelado computacional.
Esta revisión narrativa
explora el potencial transformador de estas técnicas regenerativas
emergentes, destacando su capacidad para abordar las necesidades no
cubiertas en la reparación del cartílago. Ofrecemos una visión general
actualizada de los avances en ortobiológicos y biomateriales,
centrándonos en su relevancia clínica, sus desafíos y el camino a seguir
para lograr una regeneración duradera y reproducible del cartílago.
Esta revisión integra de
forma única estrategias regenerativas de vanguardia, como la edición
genética, los andamiajes de bioingeniería y las terapias celulares
personalizadas, haciendo hincapié tanto en las innovaciones técnicas
como en las aplicaciones clínicas. Al considerar factores específicos
del paciente, como la edad, el tamaño del defecto y la accesibilidad a
la atención médica, nuestra revisión ofrece una perspectiva práctica que
no se aborda habitualmente en publicaciones similares.
Conclusiones
El panorama
en constante evolución de la reparación del cartílago se caracteriza
por la innovación continua en terapias regenerativas, incluyendo
enfoques basados en células madre, edición genética, andamiajes de
bioingeniería y técnicas avanzadas de estimulación. Si bien cada método
ha demostrado potencial individualmente, su combinación en estrategias
de tratamiento integrales y multimodales puede proporcionar resultados
clínicos más duraderos y efectivos. El desarrollo de terapias
personalizadas, guiado por los avances en genómica, ciencia de
biomateriales y bioingeniería, podría redefinir la reparación del
cartílago y la preservación articular.
La investigación futura
debe centrarse en perfeccionar los enfoques combinados, desarrollar
protocolos de tratamiento estandarizados y realizar ensayos clínicos a
largo plazo para evaluar la seguridad, la eficacia y la sostenibilidad.
La colaboración interdisciplinaria entre médicos, bioingenieros y
organismos reguladores será esencial para incorporar estas terapias
avanzadas a la práctica clínica habitual. Los modelos personalizados,
basados en datos y guiados por inteligencia artificial y algoritmos
predictivos, probablemente definirán la próxima generación de soluciones
de reparación del cartílago, mejorando en última instancia los
resultados de los pacientes y redefiniendo los estándares en la
preservación articular y el cuidado musculoesquelético.